Пересмотр диагностических критериев синдромов J-волны: новые концепции и их актуальность для практики кардиолога (по материалам экспертного согласительного документа APHRS/EHRA/HRS/SOLAEGE 2016г.)
Внезапная сердечная смерть (ВСС) является одной из ведущих причин смертности в экономически развитых странах. Частота ее развития составляет 15–20%
от всех ненасильственных случаев смерти [1]. Согласно расчетным данным, в Российской Федерации внезапно от сердечных причин ежегодно умирают 200 000–250 000 человек [2]. Наиболее активно изучаемыми в последнее время являются аритмии, связанные с мутациями в генах, которые отвечают за функционирование ионных каналов, экспрессирующихся в миокарде. Данные генетически детерминированные аритмии относят к группе каналопатий и, учитывая наличие наследственно обусловленного нарушения образования и/или распространения электрического импульса, их также называют первичными электрическими болезнями сердца [1].
Представления о механизмах развития генетически обусловленных аритмий, терминология и объем знаний настолько быстро развиваются, что приходится переоценивать данные, полученные еще несколько лет назад, в соответствии с новыми представлениями [2]. Синдром волны J – термин, включающий два синдрома: синдром Бругада (сБр) и синдром ранней реполяризации желудочков (СРРЖ) [3–5], захватил интерес кардиологического сообщества в последние два десятилетия [6], последовавшие после открытия в 1992 г. братьями Педро и Джозефом Бругада новой нозологии, идентифицированной как синдром Бругада [7].
Значение СРРЖ было объективно оценено только в 2008 г. [8, 9]. Согласительные конференции, посвященные сБр, состоялись в 2000 и 2004 гг. [10, 11]. Специальных конференций по теме СРРЖ не проводилось до уточнения вопросов, связанных с терминологией, и только в 2013 г. приняты рекомендации по обоим синдромам [12]. Появление новых знаний требовало формирования новых концепций и подходов в отношении диагностики, прогноза, клеточных и ионных механизмов, стратификации риска и подходов к терапии. Итогом конференции ведущих экспертов Общества сердечного ритма (HRS), Европейской ассоциации ритма сердца (EHRA), Азиатско-Тихоокеанского общества ритма сердца (APHRS) и Латиноамериканского общества стимуляции сердца и электрофизиологии (SOLAECE), состоявшейся в Шанхае в апреле 2015 г., явилось создание согласительного документа по проблеме синдромов J-волны,
посвященного новым концепциям и пробелам в знаниях в данной области, который был опубликован в 2016 г. [6].
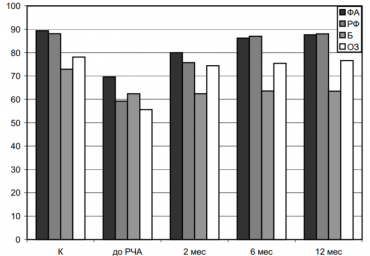
Основные положения данного документа и составляют содержание данного обзора. Буква «J» относится к точке соединения комплекса QRS и сегмента ST, представляющей переход от конца деполяризации к началу реполяризации желудочков. Волна J представляет собой хорошо выраженную позднюю положительную волну, следующую за комплексом QRS, либо зазубренность на нисходящем колене зубца R, маленький добавочный зубец r (r'), который напоминает по форме «горб верблюда» (camel-hump sign), «крючок для шляпы», «купол», «зарубку» [13] (рис. 1).
Термин «ранняя реполяризация» используется кардиологами уже на протяжении 40 лет [14]. Отсутствие согласованности относительно терминологии, связанной с ранней реполяризацией, приводившее к разночтениям в публикациях (в частности, распространенность ранней реполяризации варьирует, по различным источникам, от 2 до 31%), явилось предпосылкой для создания согласительного документа, который сфокусировал внимание на терминологии паттерна ранней реполяризации и рекомендациях по стандартизации необходимых измерений [14]. Как электрокардиографический феномен волна
J впервые описана F. Kraus в 1920 г. [15].
Появление отчетливой волны J на электрокардиограмме (ЭКГ) связывали с гипотермией [16–18] (в этом случае она называлась «волна Осборна») и гиперкальциемией [15, 19]. Клиническое и аритмогенное значение волны J в значительной степени игнорировалось до 1999 г. [20], пока G.X. Yan и C. Antzelevitch не опубликовали работу об ионных и клеточных основах волны J и механизмах аритмогенеза [21], а в 2005 г. была отмечена связь волны J
с угрожающими жизни аритмиями [22].
Синдромы волны J получили свое название в связи с тем, что характеризуются акцентуацией волны J на ЭКГ. Основой происхождения волны J является электрофизиологическое различие эпи- и эндокардиальных клеток миокарда по продолжительности потенциала действия (ПД) в ранних фазах (1-й и 2-й). Как известно, форму ПД определяют входящие натриевые (INa) и кальциевые токи (ICa) или выходящий калиевый ток (Ito) [13]. Экспериментальные исследования показали, что причиной появления волны J является трансмуральный вольтажный градиент, вызывающий манифестацию «зарубки» ПД в эпикарде (но не в эндокарде) за счет гетерогенного трансмурального распределения Ito [23].
В настоящее время принято считать, что СРРЖ и сБр представляют два варианта проявления синдрома волны J [12]. Кроме характерного ЭКГ-паттерна, оба синдрома ассоциируются с готовностью к развитию полиморфной желудочковой тахикардии (ЖТ) и фибрилляции желудочков (ФЖ), приводящих к ВСС у молодых людей без структурных заболеваний сердца [24], а также к внезапной младенческой смерти [25]. Клеточные механизмы, лежащие в основе синдрома волны J, длительное время были предметом дебатов [26]. В случае сБр выдвинуты 2 принципиальные гипотезы. Первая – гипотеза реполяризации, заключается в том, что сдвиг баланса токов к эпикарду правого желудочка (ПЖ) может привести к аномалиям реполяризации, выражающимся в развитии
re-entry 2-й фазы, и может вызвать экстрасистолы, способные индуцировать ЖТ/ФЖ. Вторая гипотеза – гипотеза деполяризации, предполагает, что замедленное проведение в выходном отделе правого желудочка (ВОПЖ) вследствие фиброза и снижения коннексина-43 приводит к прерыванию проведения, что играет первичную роль в появлении изменений на ЭКГ и аритмической манифестации синдрома [27].
Несмотря на то что сБр и СРРЖ различаются степенью выраженности и локализацией волны J на ЭКГ, принято считать, что они представляют единый спектр фенотипической экспрессии, называемой синдромом волны J [6, 24].
Крупнейшее многоцентровое международное рандомизированное исследование ISCHEMIA призвано ответить на вопрос об оптимальной стратегии лечения при стабильной ИБС на современном этапе. Цель исследования. В настоящей статье приводится краткий обзор исследования ISCHEMIA и проанализированы важнейшие исходные характеристики вклю‑ чаемых в него пациентов на примере одного российского центра. Материалы и методы. Критериями включения в исследо‑ вание служат наличие положительного стресс‑теста (в нашем центре это стресс‑эхокардиография с физической нагрузкой) с умеренным или высоким риском и подтверждение обструктивной ИБС по данным компьютерной томографической коро‑ нарографии (КТКГ).
Целью данного обзора является изучение влияния альдостерона и его антагонистов на структурное ремоделирование миокарда при ФП.
В монографии приведены сведения, касающиеся оценки хронотропной функции сердца, описаны новые методы оценки функции автоматизма синусового узла. Приведены данные по этиологии, патогенезу, классификации, клинике и диагностике дисфункций синусового узла.